바이러스 titration 이해
Protein expression, high-throughput screening, cell engineering 등 어떤 실험이든지 바이러스 titration은 성공적인 transduction을 위한 필수과정이다. Titration 통해 사용하는 바이러스 샘플의 particle 수 (또는 infectious unit)를 알 수 있고, transduction시 efficiency (eg. 얼마나 많은 바이러스가 cell에 들어 갔는지), cell에 integration 된 gene copy수가 어떻게 되는지를 계산할 수 있다. 따라서 다양한 titration 측정 방법과 이 방법들이 어떻게 서로 연관이 되는지를 이해하는 것이 중요하다.
■ Lentivirus product basic
바이러스 titration에는 일반적으로 physical titer를 측정하는 방법과 functional titer를 측정하는 방법이 있다. Physical titer는 핵산이나 단백질 양을 측정해서 바이러스 particle의 수를 결정하는 방법이고, functional titer는 실제 감염 활성을 가지고 있는 바이러스의 particle 수를 측정하는 (IFU/㎖) 것이다. 이러한 두 가지의 titration법에서 측정되는 것이 무엇인지를 이해하기 위해 아래에 lentivirus 생산 workflow를 정리하였다.
재조합 lentivirus의 backbone은 바이러스가 기능하는데 필요한 필수적인 cis-acting element를 가지고 있다. Lentivirus 실험은 이러한 backbone (expression vector)에 발현하고자 하는 유전자 서열을 cloning 하는 것으로 시작한다 (그림 1). 이후 expression vector를 바이러스 particle을 생산하기 위해 필요한 모든 단백질의 유전자가 들어 있는 packaging plasmids 와 함께 transfection 시약을 사용하여 packaging cell (보통 293T 기반의 cell)에 도입하여 바이러스를 생산할 수 있다.
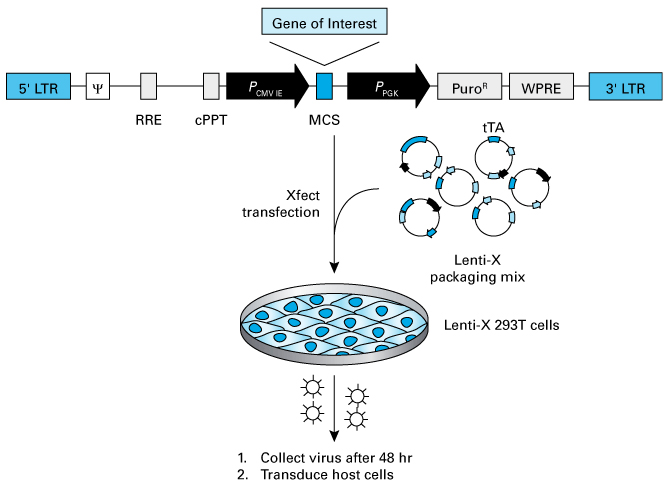 그림 1. Lentivirus 생산 workflow.
그림 1. Lentivirus 생산 workflow.
생산된 lentivirus는 세포 밖 배지로 방출되는데 여기에는 아래와 같이 (그림 2) 완전한 형태의 감염성을 가진 바이러스 외에도 감염성이 없는 바이러스와 capsid protein (예, p24)등이 포함되어 있다. Physical titration (
qRT-PCR,
p24 ELISA,
Lenti-X™ GoStix™ Plus)은 바이러스 혹은 바이러스 관련 성분을 정량하는 방법으로 비교적 간단하게 사용할 수 있는 방법이지만 감염성을 가진 바이러스 외에도 감염성을 가지고 있지 않은 다른 particle까지 검출될 가능성이 있다. 반면 functional titration은 타겟 세포에 transduction이 가능한 (예. infectious unit; IFU) 바이러스만을 특이적으로 검출하지만 직접 세포에 감염시켜 측정하므로 시간이 더 오래 걸리고 과정이 상대적으로 복잡하다 (그림 2B).
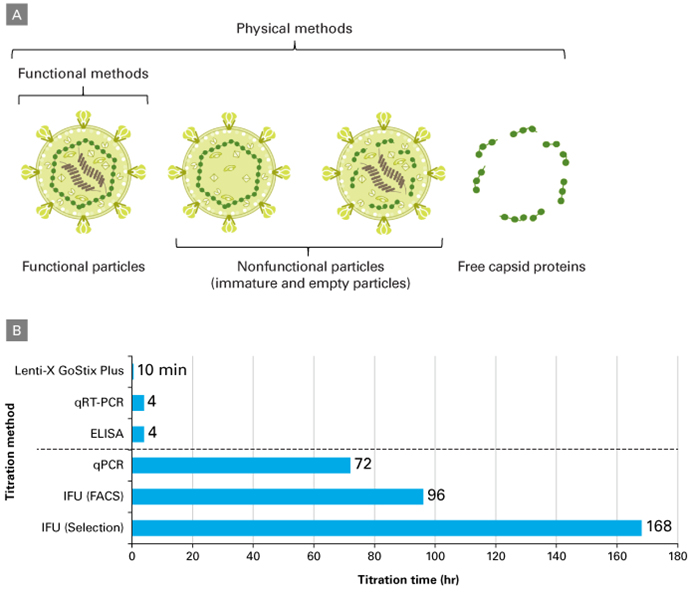 그림 2. 다양한 Titration법.
A)
그림 2. 다양한 Titration법.
A) Lentivirus 생산 후 packaging cell 배지에 있을 수 있는 여러가지 형태의 viral particle이다. physical titration은 감염성을 가지고 있는 바이러스와 감염성이 없는 바이러스 및 free capsid protein (p24)등이 같이 검출될 수 있다. 반면 functional titration법은 감염성을 가지고 있는 functional viral particle만을 특이적으로 검출한다.
B) 일반적으로 titration에 소요되는 시간을 정리한 결과이다.
- Lenti-X™ GoStix™ Plus: lateral flow 기반으로 lentivirus의 p24 capsid 단백질을 정량.
-
qRT-PCR: lentivirus의 RNA genome을 qRT-PCR로 정량.
-
ELISA: lentivirus의 p24 capsid 단백질을 ELISA로 정량
-
qPCR: 숙주 세포 genome에 삽입된 viral DNA인 provirus를 qPCR로 정량
- IFU (FACS): 형광을 이용하여 transduction 된 cell 중 positive cell을 FACS로 정량
- IFU (Selection): 항생제 저항 유전자를 이용하여 transduction된 cell의 colony 수를 정량
여기서 functional titration과 physical titration의 가장 중요한 특징이 있다. 이는 virus를 생산한 방법 (packaging system, purification/filtration법, concentration/precipitation법, harvest 시점 등)이 동일할 때 두 가지 titration법으로 측정된 결과값의 비율은 거의 유사하게 나온다는 점이다. 따라서 이 두가지 값의 계수를 구한 뒤 추후 실험에서 physical titer만 측정한 이후 functional titer로 환산하는 것이 가능하다.
■ 실험 예시
Physical titer와 functional titer 간의 계수를 한 번 계산하고 나면 상대적으로 빠르고 간편한 방법인 physical titration 방법으로도 functional titration 방법과 같은 신뢰성 높은 역가 측정이 가능하다. 아래에
Lenti-X™ GoStix™ Plus (Code 632180)로 측정된 결과를 IFU/㎖로 환산하기 까지의 과정을 예시로 제시하였다. 이 방법은
qRT-PCR법이나
ELISA법에서도 동일하게 적용이 가능하다.
GoStix™ cassette로 반응 후 전용 앱을 통해 분석하면 앱의 소프트웨어가 밴드의 밀도를 측정하고 이를 서버에 저장된 lot 별 standard curve와 비교해 샘플의 p24 capsid 단백질을 정량한다 (ng/㎖ p24). 이 결과를 functional titer로 환산하기 위해서는 동일한 reference virus를 functional titration 방법으로 측정해야 한다 (IFU/㎖). 이 두 가지 titration법으로 계산한 계수는 추후 동일한 조건으로 적용하여 physical titer를 측정한 뒤 functional titer를 환산하는데 사용할 수 있다.
Reference vector functional titer = |
2.2 x 108 IFU/㎖ |
÷Reference vector physical titer = |
525 ng/㎖ p24 |
Reference vector ratio = |
4.2 x 105 IFU/ng p24 |
Physical titer for unknown vector (measured) = |
790 ng/㎖ p24 |
X Reference vector ratio (from above) = |
4.2 x 105 IFU/ng p24 |
Functional titer for vector to be (calculated) = |
3.3 x 108 IFU/㎖ |
그림 3. Phyical titer를 functional titer로 환산하는 예시. Lenti-X™ GoStix™ Plus로 525 ng/㎖ p24가 나왔고, FACS로 2.2 x 10
8 IFU/㎖가 나왔다는 가정이다. 위의 두 값을 나누면
4.2 x 105 IFU/ng p24의 계수가 산출된다. 다음 실험에서 Lenti-X™ GoStix™ Plus로 790 ng/㎖ p24가 나왔다면 이 값에 앞에서 구한 계수인
4.2 x 105 IFU/ng p24를 곱하여 functional titer와 같은 단위인 IFU/㎖로 환산할 수 있다 (3.3 x 10
8 IFU/㎖).
■ 결론
Lentivirus의 실험에서 transduction efficiency를 확인하고, 이후 실험에 필요한 lentivirus 샘플의 양을 정확하게 계산하기 위해 titration이 꼭 진행되어야 한다. 기존에는 이중 functional titer를 측정하는 방법이 많이 사용되었으나 시간이 매우 오래 걸리고, 실험이 복잡하며, lentivirus 생산 직후 가장 functional한 상태의 바이러스의 사용이 불가능하다는 한계가 있었다. 따라서 근래에는 실험이 빠르고 간단한 physical titer를 측정하고 이 값을 functional titer로 환산하여 사용하는 방법이 많이 사용되고 있다.
■ 추천하는 Lentivirus titration 시스템
- Lentivirus 전체 실험 workflow 별 추천 제품
보러가기





