- 고객지원
- 업무안내│제품문의
- 전화번호│02-2081-2510
- Email │support@takara.co.kr
- 대전지사
- 업무안내│대전/충청지역 주문, 제품문의
- 전화번호│042-828-6525
- Email │tkbd@takara.co.kr
- 업무시간안내
- [ 평 일 ] 09 : 00 ~ 18 : 00 │ [ 점심시간 ] 12 : 00 ~ 13 : 00
- 토·일요일, 공휴일은 휴무입니다.
Center for Gene and Cell Processing (CGCP)
GMP시설에서 진행되는 Gene and Cell Processing Custom Service※본 서비스는 모두 Takara Bio Inc.(Japan)에서 진행되며, 본 소개에 사용된 자료는 Takara Bio Inc.에서 저작권을 가지고 있음을 알려드립니다.
다카라바이오㈜는 유전자 의료(유전자치료, 세포의료)사업의 상용화 및 바이오 의약품과 재생의료/세포의료 지원 서비스에 보다 더 매진하기 위해
대규모 유전자·세포 처리센터 CGCP (Center for Gene and Cell Processing)를 개설하였습니다.
본 센터에서는 GMP/GCTP 관리하에 유전자 의료에
대한 최첨단 설비와 노하우를 살려, 유전자 치료와 세포의료 등의 첨단 의료를 지원합니다.
[시설 개요]
대규모 GMP/GCTP 지원시설인 CGCP(Center for Gene and Cell Processing)는 유전자 의료(유전자 치료, 세포 의료 등)를 위한 각종 Cell Banking, 유전자 의료용 vector 제작, 세포 가공 등의 시험용 신약을 GMP 기준에 따라 제조 할 수 있습니다. 기타 품질 시험 및 특성 분석, 보관 서비스도 시행하고 있으며, 유전자 치료 프로젝트의 기반 기술 개발과 아울러 임상 개발의 베스트 파트너로서 고객을 지원합니다.

[Facility of the Year Awards 수상]
국제제약기술협회 (International Society for Pharmaceutical Engineering, Inc. : ISPE)에서 시상하는 2016년 Facility of the Year Awards(FOYA)의 설비통합(Facility Integration) 부문을 수상하였습니다. Facility of the Year Awards(FOYA)는 2005년에 설립된 시상으로, 혁신적인 기술로 설계, 건설, 운영되고 있는 의약품이나 의료 기기의 제조/개발 시설에 수여됩니다. 총 6개 부문에서 시상되는 본 상 중에 설비 통합 부문에서의 다카라바이오 CGCP의 수상은 CDMO 사업에서 꼭 필요한 재생의료용 제품 등을 안전하고 효율적으로 제조할 수 시설로서의 설계, 운영, 환경 등의 측면에서 조화로운 점이 높은 점수를 받았습니다.





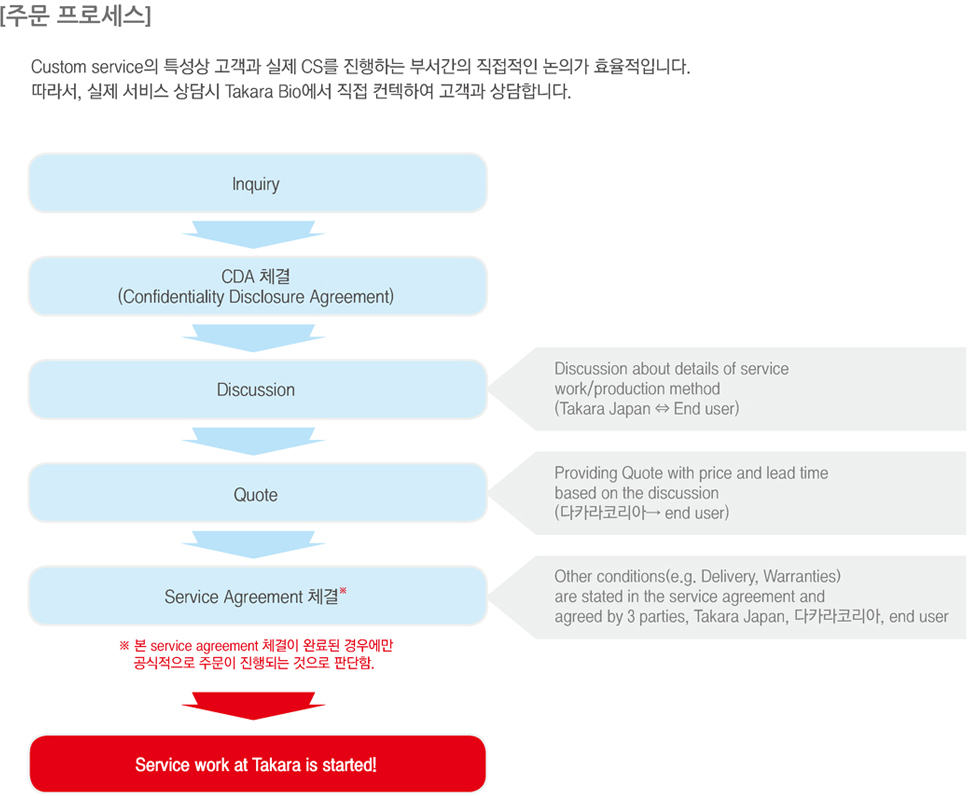
한국내 서비스의뢰에 대한 자세한 문의는 다카라코리아 고객지원센터(02-2081-2510, support@takara.co.kr)로 연락바랍니다.

[시설 개요]
대규모 GMP/GCTP 지원시설인 CGCP(Center for Gene and Cell Processing)는 유전자 의료(유전자 치료, 세포 의료 등)를 위한 각종 Cell Banking, 유전자 의료용 vector 제작, 세포 가공 등의 시험용 신약을 GMP 기준에 따라 제조 할 수 있습니다. 기타 품질 시험 및 특성 분석, 보관 서비스도 시행하고 있으며, 유전자 치료 프로젝트의 기반 기술 개발과 아울러 임상 개발의 베스트 파트너로서 고객을 지원합니다.

[Facility of the Year Awards 수상]
국제제약기술협회 (International Society for Pharmaceutical Engineering, Inc. : ISPE)에서 시상하는 2016년 Facility of the Year Awards(FOYA)의 설비통합(Facility Integration) 부문을 수상하였습니다. Facility of the Year Awards(FOYA)는 2005년에 설립된 시상으로, 혁신적인 기술로 설계, 건설, 운영되고 있는 의약품이나 의료 기기의 제조/개발 시설에 수여됩니다. 총 6개 부문에서 시상되는 본 상 중에 설비 통합 부문에서의 다카라바이오 CGCP의 수상은 CDMO 사업에서 꼭 필요한 재생의료용 제품 등을 안전하고 효율적으로 제조할 수 시설로서의 설계, 운영, 환경 등의 측면에서 조화로운 점이 높은 점수를 받았습니다.

Virus vector 제조 및 생산서비스
다양한 종류의 바이러스 vector 제작 및 바이러스 생산
다양한 종류의 바이러스 vector 제작 및 바이러스 생산
유전자 의료용 바이러스(virus) vector 생산을 위한 제조실 및 정제실을 별도로 보유하고 있으며, 각종 바이러스 vector 제작이 가능합니다.
다카라바이오는 오랜 유전자 치료 개발 프로젝트를 진행해 오면서, 많은 바이러스 vector GMP 제조 경험을 가지고 있습니다. CGCP에서는
그 생산 규모를 확장하고 축적된 경험과 노하우를 살린 서비스를 제공합니다.
| ◆ Retrovirus | ◆ Herpes Simplex virus | |
| ◆ Adeno-associated virus | ◆ Lentivirus | |
| ◆ Sendai virus 외 |

Cell Processing 서비스
특정 세포 선별 및 특정유전자 삽입, 확대 배양 서비스
특정 세포 선별 및 특정유전자 삽입, 확대 배양 서비스
독립적인 Cell Processing 공간을 확보하고 있으며, iPSC 를 포함한 master cell bank (MCB)제작 및
가공이 가능하며, 특정 세포 가공 및 재생 의료 등의 제품을 생산할 수 있습니다.
세포 배양 조건 검토부터 대량 배양까지 종합적으로 지원할 수 있는 체제 및 설비를 갖추고 있으며, 연구용은 물론, 임상 시험의 각 단계에서 원하는 관리 기준하에서 세포 가공 및 배양을 할 수 있습니다.
연간 약 200 ~ 2,400 batch의 세포 조제가 가능합니다.
세포 배양 조건 검토부터 대량 배양까지 종합적으로 지원할 수 있는 체제 및 설비를 갖추고 있으며, 연구용은 물론, 임상 시험의 각 단계에서 원하는 관리 기준하에서 세포 가공 및 배양을 할 수 있습니다.
연간 약 200 ~ 2,400 batch의 세포 조제가 가능합니다.

품질 검사 및 특성분석시험
무균시험 및 mycoplasma 검사
무균시험 및 mycoplasma 검사
CGCP의 품질 검사실에서는 무균시험(sterility test) 및 mycoplasma 테스트 (배양법, DNA 염색법)를
일본 약전에 따라 실시하고 있습니다. 양성 균주를 이용한 저해 확인검사도 가능합니다. 또한 endotoxin 검사와 qPCR을 이용한 mycoplasma 테스트 및 바이러스 검사를
실시하고 있습니다.
기타 특성분석시험 (세포표면 항원측정, cytotoxicity 활성측정, cytokine 측정, 감염 역가 측정, 제조공정유래 불순물검사 등)도 가능하니, 문의바랍니다.
본 서비스는 Viral vector manufacturing, cell processing 등 수탁시 quality test용으로 진행됩니다.
기타 특성분석시험 (세포표면 항원측정, cytotoxicity 활성측정, cytokine 측정, 감염 역가 측정, 제조공정유래 불순물검사 등)도 가능하니, 문의바랍니다.
본 서비스는 Viral vector manufacturing, cell processing 등 수탁시 quality test용으로 진행됩니다.

Cell banking 서비스 (GMP grade)
다양한 세포(대장균, 포유류 세포) banking 서비스
다양한 세포(대장균, 포유류 세포) banking 서비스
Cell bank등 주요 원자재 전용보관실을 별도로 설치하여 다양한 요구에 대응하고 있습니다.
각 공간은 관계자만 출입 가능하도록 하여, 엄중한 보안 아래 보관 관리하고 있습니다.
액체질소 자동공급장치, 온도 모니터링, 온도 이상을 24 시간 감시하는 시스템을 도입하여, 고객의 세포와 중요한 대상 품목을 책임지고 보관합니다.
또한, CHO, 293 등을 비롯한 동물 세포의 셀 뱅크를 제작할 수 있으며, Research Cell Bank(RCB) 제작부터 Master Cell Bank(MCB), Working Cell Bank(WCB) 제작 등에 유연하게 대응할 수 있습니다.
단, 특정 strain은 서비스가 불가한 경우가 있으므로 문의바랍니다.
액체질소 자동공급장치, 온도 모니터링, 온도 이상을 24 시간 감시하는 시스템을 도입하여, 고객의 세포와 중요한 대상 품목을 책임지고 보관합니다.
또한, CHO, 293 등을 비롯한 동물 세포의 셀 뱅크를 제작할 수 있으며, Research Cell Bank(RCB) 제작부터 Master Cell Bank(MCB), Working Cell Bank(WCB) 제작 등에 유연하게 대응할 수 있습니다.
단, 특정 strain은 서비스가 불가한 경우가 있으므로 문의바랍니다.
액체 질소 자동 공급 장치 ->


한국내 서비스의뢰에 대한 자세한 문의는 다카라코리아 고객지원센터(02-2081-2510, support@takara.co.kr)로 연락바랍니다.