- 고객지원
- 업무안내│제품문의
- 전화번호│02-2081-2510
- Email │support@takara.co.kr
- 업무시간안내
- [ 평 일 ] 09 : 00 ~ 18 : 00 │ [ 점심시간 ] 12 : 00 ~ 13 : 00
- 토·일요일, 공휴일은 휴무입니다.
- OEM
- Gene and cell therapy manufacturing
- PRTSS
임상용 Viral Vector 생산 서비스

Takara Bio의 Clinical-grade Viral Vector Production 서비스는 10년 이상의 경험을 바탕으로 유전자치료제 및 세포치료제 임상 개발을 위한 고품질 viral vector (AAV, Lentivirus 등)를 GMP 기준에 맞춰 생산·공급합니다.
서비스 개요
Takara Bio는 Adeno-associated virus (AAV), lentiviral vector, retroviral vector에 대한 생산 서비스를 제공합니다. 기술 이전을 통해 다른 viral vector도 생산 가능합니다.
아래 영상에는 당사의 small scale 및 large scale viral vector manufacturing workflow에 대한 모든 정보를 담았습니다.
당사의 원스톱 GMP 제조 시설은 개발 초기 단계의 소규모 시제품 제조부터 최대 2,000L 규모의 대규모 제조까지 광범위한 생산 스케일을 지원할 수 있습니다.
의뢰한 viral vector의 보다 더 효율적인 생산을 위하여, 필요한 생산 조건등의 조정을 위해 소규모(small scale) 제조부터 시작하시는 것을 권장합니다. 필요할 경우, 특정 배양 용기(culture vessels) 또는 최종 제품 용기(containers, 특정 vials 혹은 bags)에 대해서도 선택가능합니다.
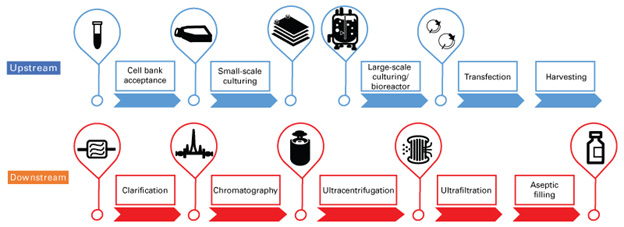
[그림] Viral vector manufacturing workflow
Adeno-associated virus (AAV)
AAV vector는 증식하는 세포에 유전자를 전달하고 장기간 발현을 유도할 수 있습니다. 또한, AAV vector는 면역원성이 매우 낮아, 유전자 치료에 대한 적용성이 매우 높아지고 있습니다. 다양한 혈청형 (serotype)은 서로 다른 특성과 조직 특이성을 나타내므로, AAV vector는 심장, 간, 근육, 망막 및 중추신경계 조직에 표적 유전자를 효율적으로 전달할 수 있습니다.
- Project initiation: plasmid DNA (transfer plasmid, packaging plasmids)와 producer cell line 제공
- New! Takara Bio는 유전자 치료제에 최적인 vector CereAAV™를 제공합니다. CereAAV™는 유전자 공학 및 독자적인 스크리닝 기술을 통해 뇌 친화성을 향상시킨 AAV2-based serotype입니다. 연구 결과에 따르면 CereAAV™는 AAV9에 비해 마우스에서 50배, 영장류 모델(예: 마모셋)에서 20배 높은 유전자 전달 효율을 보이고 있습니다. - Deliverables: AAV vector, manufacturing report, certificate of analysis
AAV vector productionTime (months; varies with project scope) |
||||||||||||
Workflow |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
20 |
22 |
24 |
MCB manufacturing (GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
Quality testing for MCB (GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
Process development/AAV test batch (non-GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
Evaluation by customer |
|
|
|
|
|
|
|
|
|
|
|
|
AAV test batch (non-GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
AAV manufacturing (GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
Quality testing for AAV (GMP) |
|
|
|
|
|
|
|
|
|
|
|
|
Examples of standard QC tests for an AAV vector |
||
Quantitative/functional tests |
Purity tests |
Safety tests |
Gene expression |
Host cell protein |
Sterility |
Vector sequence |
Host cell DNA |
Mycoplasma |
Viral titer (qPCR or ddPCR) |
|
Endotoxin |
|
|
Replication-competent AAV |
Lentivirus
Lentiviral vector는 복제 세포와 비복제 세포 모두에 유전자를 전달할 수 있습니다. 일반적으로 retrovirus보다 높은 역가로 생산되며, 숙주 게놈에 끼어들어 형질전환 유전자의 안정적이고 장기적인 발현을 가능하게 합니다. 또한, lentiviral vector는 상대적으로 낮은 면역 반응을 유발하므로 유전자 치료에 널리 사용됩니다.
- Project initiation: plasmid DNA (transfer plasmid, packaging plasmids)와 producer cell line(293T MCB는 요청에 따라 당사 제공가능) 제공
- Takara Bio 고유의 다양한 pLVpro vector 가 포함된 LVpro Packaging Mix를 사용할 수 있으며, 임상 사용에 적합한 lentivirus plasmid vector가 필요하시면 문의해 주십시오. - Deliverables: Lentiviral vector, manufacturing report, certificate of analysis
Lentiviral vector productionTime (months; varies with project scope) |
|||||||||||||
Workflow |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
20 |
22 |
24 |
|
Manufacturing of MCB (GMP) |
|
|
|
|
|
|
|
|
|
|
|
||
Quality testing for MCB (GMP) |
|
|
|
|
|
|
|
|
|
|
|||
Process development/lentiviral vector small-scale test batch (non-GMP) |
|
|
|
|
|
|
|
|
|
|
|||
Evaluation by customer |
|
|
|
|
|
|
|
|
|
|
|
||
Lentiviral vector test batch (non-GMP) |
|
|
|
|
|
|
|
|
|
|
|||
Lentiviral vector manufacturing (GMP) |
|
|
|
|
|
|
|
|
|
|
|
||
Quality testing for lentiviral vector (GMP) |
|
|
|
|
|
|
|
|
|
|
|||
Examples of standard QC tests for a lentiviral vector |
||
Quantitative/functional tests |
Purity tests |
Safety tests |
Gene expression |
Host cell protein |
Sterility |
Vector sequence |
Host cell DNA |
Mycoplasma |
Viral titer |
|
Endotoxin |
|
|
Replication-competent lentivirus |
Retrovirus
Retroviral vector는 감염시키기 어려운 다양한 분열 세포를 형질전환 시키고, 숙주 게놈에 끼어들어, 유전자를 장기간 안정적으로 발현시키는 데 이상적입니다.
- Project initiation: plasmid DNA and a packaging cell line (PG13 packaging cell line은 요청시 당사 제공가능)
- Deliverables: Master Cell Bank (MCB), retroviral vector, manufacturing report, certificate of analysis
서비스 프로세스 등 자세한 문의는 왼쪽 문의 form을 이용하거나, oem@takara.co.kr로 메일을 보내주세요.